Científicos del Instituto de Investigaciones Biomédicas Sols-Morreale (CSIC-UAM) han creado un biobanco de cultivos celulares 3D, tanto normales como tumorales de colon y recto, a partir de biopsias de más de 150 personas con cáncer colorrectal. Se trata de una vía novedosa para estudiar la enfermedad y aproximarse a la medicina personalizada, según nos cuentan dos miembros del equipo.
La investigación en biomedicina se basa en gran medida en sistemas modelo para descifrar procesos biológicos, identificar biomarcadores y desarrollar nuevas terapias. Tradicionalmente, se han utilizado animales de laboratorio y líneas celulares establecidas, sin embargo, estos sistemas no siempre reproducen adecuadamente la situación in vivo.
En este contexto surge la utilidad de los organoides: cultivos celulares tridimensionales (3D) generados a partir de células troncales –comúnmente llamadas madre–, bien multipotentes (“adultas”, presentes en los tejidos) o pluripotentes (embrionarias o inducidas mediante reprogramación genética, capaces de generar diversos tipos celulares).
Este modelo celular 3D es “uno de los más parecidos a un tejido sano y a un tejido tumoral”, señala Antonio Barbáchano, investigador del Instituto de Investigaciones Biomédicas Sols-Morreale (IIBM), un centro mixto del CSIC y la Universidad Autónoma de Madrid (UAM).
Barbáchano es experto en cáncer de colon y en el establecimiento y manejo de organoides desde que en 2011 el grupo de Cáncer de Colon del IIBM, coordinado por Alberto Muñoz, María Jesús Larriba y José Manuel González-Sancho, apostara por esta nueva línea de investigación. Con el objetivo de avanzar en esa dirección, Barbáchano realizó una estancia en el laboratorio de Eduard Batlle del Instituto de Investigación de Biomedicina (IRB Barcelona), que es líder en el campo de los organoides.

Organoides de colon en cultivo en el laboratorio del Instituto de Investigaciones Biomédicas Sols-Morreale. / IIBM
El investigador explica que los organoides derivados de tejido sano adyacente al tumor son considerados miniórganos “ya que, gracias a su capacidad de autoorganización y de diferenciación, generan estructuras muy similares al tejido del que proceden”.
Esto ha permitido crecer el epitelio intestinal en el laboratorio, algo que antes era imposible y ha supuesto avances extraordinarios en la comprensión de la biología de este tejido.
Los organoides derivados de tumores son una representación más fiel del tumor presente en el paciente (mismo patrón mutacional y morfología) que las líneas celulares establecidas.
Además, se pueden expandir y mantener de forma indefinida, permitiendo probar en ellos diferentes fármacos para determinar su efectividad directamente en las células obtenidas del paciente.
Este modelo presenta diversas ventajas frente a los cultivos tradicionales de líneas celulares en 2D, según destaca Barbáchano: “Representa mejor la realidad del paciente y permite reducir el uso de animales en experimentación. Así, esta metodología supone un avance en la investigación biomédica, ofreciendo un modelo más relevante y éticamente aceptable para estudiar enfermedades, evaluar fármacos, desarrollar terapias de precisión y avanzar en medicina regenerativa”.

Este modelo celular 3D representa mejor la realidad del paciente y permite reducir el uso de animales en experimentación

El grupo de Cáncer de Colon, perteneciente también al CIBER de Cáncer y al Instituto de Investigación Sanitaria del Hospital Universitario La Paz (IdiPAZ), ha generado en los últimos años un importante biobanco de organoides derivados de tejido sano y tumoral de colon y recto de pacientes con cáncer colorrectal, lo que supone una herramienta de gran valor para desarrollar sus propias investigaciones y para establecer colaboraciones.
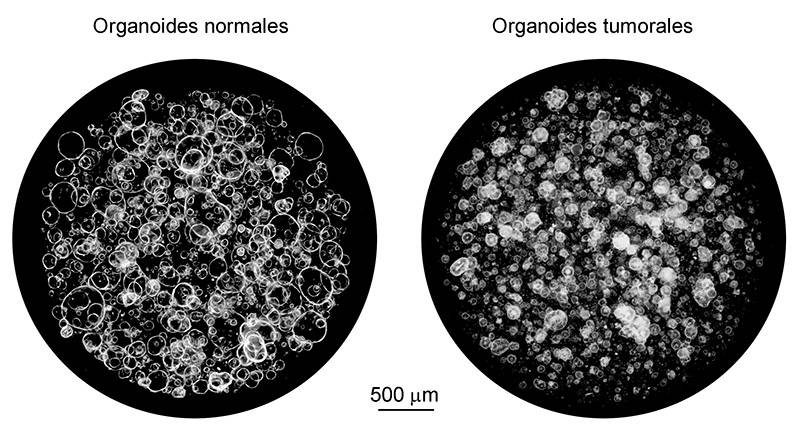
Imágenes de microscopía óptica de organoides normales y tumorales de colon derivados de pacientes con cáncer colorrectal. / IIBM
“Un ejemplo del uso de organoides para el desarrollo de nuevos agentes terapéuticos es nuestra reciente colaboración con el equipo de Atanasio Pandiella, del Centro de Investigación del Cáncer en Salamanca (CIC, CSIC-USAL)”, explica Barbáchano.
“Los utilizamos para probar un fármaco antitumoral diseñado por su grupo de investigación –añade–, que está dirigido a una proteína sobreexpresada en tumores de colon. Los ensayos mostraron una mayor toxicidad en organoides tumorales que en los normales, confirmando la eficacia del fármaco”.
Barbáchano enfatiza la ventaja de trabajar junto al Hospital Universitario La Paz, ubicado muy próximo al Campus de Medicina de la UAM, donde se encuentra el IIBM y que acogerá la futura Ciudad de la Salud de la Comunidad de Madrid. “Esta cercanía permite mantener una colaboración entre clínicos e investigadores biomédicos esencial para los proyectos con organoides”, destaca el científico.
Esta red colaborativa también integra al Hospital Universitario Fundación Jiménez Díaz, además de contar con la ayuda de la gran concienciación de la ciudadanía.
"Prácticamente todos los pacientes consultados han colaborado con la investigación. España es uno de los países del mundo donde la mayoría de los pacientes aprueban ceder parte del tejido sobrante tras la cirugía a investigación", celebra el investigador, consciente de los problemas que se presentan en otros países.
Para generar estos organoides se debe recrear en el laboratorio el nicho o microambiente en el que residen las células troncales en el organismo.
Estos nichos son zonas concretas presentes en todos los tejidos, compuestas por un microentorno especializado, altamente regulado mediante interacciones entre distintos tipos celulares y bajo la influencia de factores solubles y de la matriz extracelular, donde las células troncales permanecen en un estado indiferenciado y autorenovable.
Para el establecimiento y cultivo de los organoides, se imita el nicho embebiendo las células troncales obtenidas de la biopsia del paciente en una matriz extracelular que actúa como soporte. Esta matriz se cubre con un medio de cultivo específico que favorece el crecimiento de las células troncales.
Sin embargo, el sistema de los organoides tiene limitaciones, como reconoce Asunción Fernández-Barral, profesora de la UAM e investigadora del grupo del IIBM: “Trabajar con ellos supone una inversión económica y de tiempo considerable, mucho mayor que la que se necesita para utilizar cultivos celulares en 2D. Otras limitaciones son, por ejemplo, que la matriz extracelular utilizada tiene un origen animal, lo que complica su uso en medicina regenerativa”.
Además, precisa Fernández-Barral, “los organoides más utilizados hasta ahora están formados únicamente por células epiteliales. Su carácter puramente epitelial hace que no representen al 100 % el órgano de origen, en el que también existe tejido conectivo (estroma), sistema inmune, etc.”.
Para solventar este problema, varios laboratorios están centrados en cocultivar organoides epiteliales con otros tipos celulares (cultivos heterotípicos), como fibroblastos o células del sistema inmune, o en fusionar organoides de distintos tipos celulares, denominados asembloides.

Asunción Fernández-Barral y Antonio Barbáchano, expertos en el cultivo de organoides de colon. / IIBM
Más allá de esas limitaciones, los organoides facilitan la colaboración entre grupos de investigación. “Nuestro biobanco nos permite colaborar con grupos interesados en realizar ensayos en cultivos derivados de pacientes como una aproximación real a la medicina personalizada, pero que debido a los necesarios circuitos hospitalarios y a la alta especialización requerida para manejar los cultivos de organoides, no pueden establecerlos de rutina en sus laboratorios”.

Nuestro biobanco nos permite colaborar con grupos interesados en realizar ensayos en cultivos derivados de pacientes como una aproximación real a la medicina personalizada

Fernández-Barral confía en un futuro en el que los organoides sean de uso rutinario en los hospitales y permitan ensayar diferentes tratamientos antes de decidir cuál puede ser el más conveniente para el paciente, evitando la administración de terapias no efectivas y reduciendo así su sufrimiento y el gasto para el sistema nacional de salud.
“Todavía estamos en los inicios, pero ya se ha demostrado su gran utilidad en la selección de agentes quimioterápicos e inmunoterapias, dado que algunos estudios han mostrado que aquellos agentes que no presentan actividad en los organoides tampoco tienen efecto en los pacientes”, concluye la investigadora.
Contenido realizado dentro del Programa de Ayudas CSIC – Fundación BBVA de Comunicación Científica, Convocatoria 2022.