Científicos del CNIC han descubierto en ratones un sistema que puede promover la arterialización y perfusión en los tejidos que han sufrido una reducción del riego sanguíneo. El estudio, publicado en Nature, propone que el bloqueo selectivo de la proliferación y el metabolismo celular mejora la vascularización terapéutica en la enfermedad cardiovascular.
Una investigación llevada a cabo por científicos del Centro Nacional de Investigaciones Cardiovasculares (CNIC), liderados por Rui Benedito, ha dado un gran paso en la comprensión de la biología de los vasos sanguíneos. Además, sus resultados permitirán diseñar mejores estrategias terapéuticas para inducir una vascularización y perfusión más efectiva en tejidos lesionados o isquémicos.
El estudio, publicado en Nature, describe un nuevo mecanismo celular y molecular que es esencial para el desarrollo de arterias a partir de capilares sanguíneos, un proceso biológico llamado arterialización. La activación de este sistema en los tejidos que han sufrido una reducción transitoria o permanente del riego sanguíneo –como ocurre tras un infarto de miocardio– podría mejorar la regeneración y función del tejido cardiaco.
Hasta ahora se pensaba que este proceso de arterialización dependía de la diferenciación y especificación de una célula progenitora en una célula arterial, proceso que se producía mediante la activación transcripcional y remodelado del ADN. Sin embargo, este trabajo muestra que requiere la supresión del metabolismo y progresión del ciclo celular, un evento necesario para desencadenar una diferenciación y desarrollo arterial adecuados.
En los últimos 20 años, los científicos han descubierto diferentes mecanismos celulares y moleculares que son esenciales para la formación y diferenciación de las arterias y las venas. “Los primeros vasos sanguíneos que se desarrollan en cualquier órgano en crecimiento son inicialmente inmaduros y forman una red vascular indiferenciada y rudimentaria”, explican los expertos del CNIC.
Esta red o plexo vascular precursor está formada por células endoteliales y es relativamente poco eficaz a la hora de transportar la sangre. Sin embargo, gracias a la acción concertada de varias vías genéticas –incluidas las vías de señalización del receptor Notch y del factor de crecimiento endotelial vascular (VEGF)– se inicia la diferenciación y movilización de un subconjunto de células en estos vasos rudimentarios para formar las futuras arterias y venas.
Los autores explican que la formación de un sistema vascular jerárquico compuesto por vasos conductores más grandes resulta esencial para transportar la sangre de manera eficiente dentro y fuera de los tejidos.
“Un fallo en este sistema es la causa de muerte embrionaria prematura o de distintas enfermedades potencialmente mortales por malformaciones vasculares que pueden provocar desde un accidente cerebrovascular, una reducción en el aporte de oxígeno o una mala perfusión tisular”, aseguran.
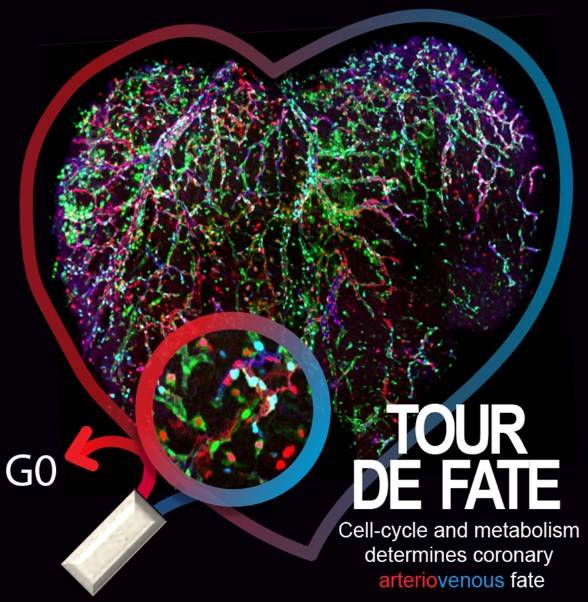
Imagen de un corazón de ratón en la que se indujo un mosaico genético multiespectral en vasos coronarios. Esta nueva tecnología genética y de imagen se utilizó para inducir distintas mutaciones genéticas y el etiquetado de células endoteliales coronarias individuales para así mapear su destino durante el desarrollo vascular. Estas mutaciones inhiben o promueven la progresión del ciclo celular, y así determinan su destino arterial o venoso. Las células necesitan salir del ciclo celular (G0) para formar arterias. / CNIC
Para que se inicie una correcta especificación arterial es preciso que, inicialmente, se produzcan dos eventos: la activación de VEGF y de la vía de señalización de Notch. “Notch es un sistema de señalización celular capaz de regular directamente la transcripción de una inmensa variedad de genes que alterarán la biología de una célula. Cuando esta vía no se activa en las células endoteliales, se produce el fallo de la especificación arterial y de su desarrollo y, por ello, solo se pueden formar células endoteliales capilares y venosas”, explica Benedito.
Esto llevó a la opinión de que las arterias se constituyen mediante la inducción de un programa de cambio genético arterial altamente conservado y dependiente de Notch en un subconjunto de células endoteliales. Se pensaba que dicho programa genético era esencial para que las células endoteliales se diferenciaran, migraran y formaran arterias.
Gracias al uso de modelos genéticos de ratones de imagen y mapeado celular (fate mapping), el grupo de Benedito ha desvelado que las células con distintos niveles de señalización Notch están sesgadas, pero no genéticamente predeterminadas, ya que pueden adoptar distintos destinos arteriovenosos si se encuentran en un contexto biofísico adecuado.
Wen Luo, primer autor del estudio, descubrió que la función principal de VEGF y Notch en las células endoteliales sometidas a arterialización es inhibir Myc y su papel promotor del ciclo y metabolismo celular, y que dicha inhibición por sí solo puede inducir un sesgo efectivo en la arterialización.
Los resultados tienen importantes implicaciones en cuanto al uso de compuestos farmacológicos dirigidos a estimular la angiogénesis –formación de los vasos sanguíneos– en la enfermedad isquémica cardiovascular.
Así, el estudio sugiere que los fármacos proangiogénicos que estimulan la proliferación general de vasos sanguíneos suprimirían la arterialización. “La clave ahora será identificar nuevas formas de eliminar las señales de proliferación exclusivamente en las células prearteriales, para así poder inducir una arterialización eficaz al mismo tiempo que se promueve la angiogénesis capilar”, añade Benedito.
Los investigadores aseguran que la capacidad de modular la identidad arterial o venosa de los vasos sanguíneos es de gran interés para el tratamiento de la enfermedad arterial coronaria y la isquemia del miocardio. “Los resultados obtenidos pueden permitir una mejor inducción del proceso de arterialización durante el crecimiento o regeneración tisular o en la enfermedad cardiovascular isquémica”, concluyen.
Referencia:
Wen Luo, Rui Benedito et al.: Arterialization requires the timely suppression of cell growth. Nature doi: 10.1038/s41586-020-3018-x
La investigación ha recibido financiación del European Research Council (ERC) Starting 880 Grant AngioGenesHD (638028).