Variantes del gen CYP3A4 están asociadas a la aparición de neuropatía periférica, la toxicidad más frecuente y limitante en los pacientes que reciben quimioterapia con paclitaxel, que incluye hormigueo y dolor en las extremidades, calambres, debilidad muscular y dificultad para caminar. El hallazgo permitiría individualizar las terapias en las personas afectadas.
El paclitaxel es un fármaco quimioterapéutico que ha demostrado una alta eficacia en el tratamiento de tumores sólidos como los de mama, ovario y pulmón. Sin embargo, su uso causa con frecuencia neuropatías periféricas, unos problemas neurológicos que afectan a la gran mayoría de los pacientes y que incluyen síntomas como hormigueo y dolor en las extremidades, calambres, debilidad muscular y dificultad para caminar, entre otros.
En ocasiones la severidad de estos efectos adversos obliga a la reducción de la dosis e incluso a la suspensión del tratamiento. Es más, en los casos más extremos, estos síntomas son irreversibles y se mantienen de por vida, disminuyendo la calidad de vida de los pacientes.
El riesgo individual de los pacientes a desarrollar neuropatía periférica por paclitaxel es desconocido. Hasta la fecha otros estudios habían sugerido la existencia de variantes genéticas que podrían aumentar la susceptibilidad de sufrir este trastorno, aunque no existía ningún marcador clínico predictivo de su aparición.
Ahora, científicos del Centro Nacional de Investigaciones Oncológicas (CNIO) han identificado, en colaboración con el Instituto Karolinska de Suecia, un primer marcador genético vinculado a la toxicidad neurológica severa. Los resultados podrían ser muy valiosos en la práctica clínica hospitalaria, puesto que ayudarían a evaluar los riesgos del tratamiento de forma individualizada y mejorar así la calidad de vida de los pacientes portadores de estas variantes.
Los autores añaden que esta información podría ser especialmente valiosa en la población española: “A pesar de que se trata de variantes poco frecuentes o raras en la población, su frecuencia es mayor en España que otros países”. Hasta uno de cada 35 españoles porta en su genoma alguna de estas variantes genéticas.
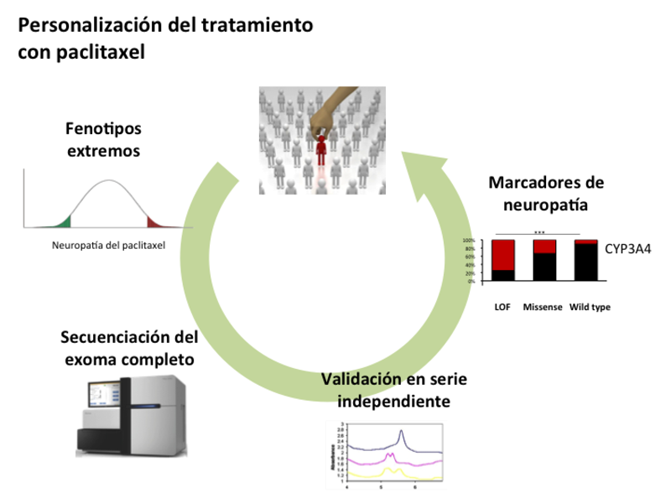
Diseño del estudio que ha identificado las variantes del gen CYP3A4 asociadas a la neuropatía severa del paclitaxel. / CNIO
El estudio, liderado por Cristina Rodríguez-Antona, investigadora del grupo de cáncer endocrino hereditario del CNIO, dirigido por Mercedes Robledo, se recoge en la revista Clinical Cancer Research.
Excreción del fármaco reducida, mayor toxicidad
Inicialmente, los investigadores secuenciaron el exoma —la parte del genoma que se traduce a proteínas— completo de ocho pacientes españolas con cáncer de mama, que habían desarrollado neuropatías extremas tras haber sido tratadas con paclitaxel.
En esta primera fase de la investigación, descubrieron unas variantes genéticas asociadas a la pérdida de función de la enzima hepática CYP3A4, que se encarga de eliminar el fármaco del organismo.
“Ante estos resultados, analizamos genéticamente una población independiente de 228 pacientes españolas tratadas con este mismo fármaco, en busca de estas variantes. El estudio nos confirmó su presencia en las pacientes con mayor toxicidad”, dice Rodríguez-Antona.
La enzima CYP3A4 está involucrada en el metabolismo de más del 50% de los fármacos actualmente utilizados en clínica. La investigadora explica que, “por este motivo, identificar a los pacientes que portan estas variantes que disminuyen su actividad es crucial para optimizar los tratamientos, especialmente los que se llevan a cabo con fármacos en los que la diferencia entre la dosis terapéutica y la que produce toxicidad es muy pequeña, como es el caso de los utilizados en oncología”.
Todavía no se conocen todas las causas que provocan el desarrollo de neuropatías periféricas durante el tratamiento con paclitaxel, pero los resultados de este estudio apuntan a la importancia de realizar cribados que detecten variantes de pérdida de función de CYP3A4 en pacientes tratados con este fármaco.
“Nuestra investigación demuestra que las tecnologías de secuenciación del exoma completo, de reciente desarrollo, pueden ser empleadas para identificar marcadores genéticos que influyen en la aparición de efectos adversos a fármacos”, concluye.
Referencia bibliográfica:
María Apellániz-Ruiz, Mi-Young Lee, Lara Sánchez, Gerardo Gutiérrez-Gutiérrez, Isabel Calvo, Laura García-Estévez, María Sereno, Jesús García-Donás, Beatriz Castelo, Eva Guerra, Luis J. Leandro-García, Alberto Cascón, Inger Johansson, Mercedes Robledo, Magnus Ingelman-Sundberg, Cristina Rodríguez-Antona. Whole-exome sequencing reveals defective CYP3A4 variants predictive of paclitaxel dose-limiting neuropathy. Clinical Cancer Research (2014). doi: 10.1158/1078-0432.CCR-14-1758
El estudio ha sido financiado por el Ministerio de Economía y Competitividad, The Swedish Cancer Foundation, The Swedish Research Council y el Instituto Karolinska de Suecia.